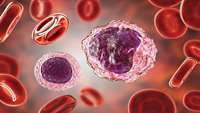
استفاده زودهنگام از محصولات تاییدشده مبتنی بر CAR T-Cell برای درمان مولتیپل میلوما بجای بکارگیری آن ها در خط پایانی درمان
سازمان غذا و دارو آمریکا درمان CAR T-Cell تراپی با کمک Abecmaرا به عنوان درمان خط دوم و درمان Carvykti را به عنوان درمان خط سوم برای مولتیپل میلوما تایید کرده است و انجمن پیوند و سلول درمانی آمریکا (ASTCT)حمایت خود را از این مسئله اعلام کرده است.
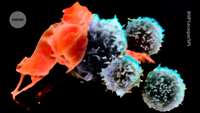
اولین سلول درمانی مبتنی بر لنفوسیت های نفوذ کننده به تومور برای درمان تومورهای جامد وارد کلینیک شد
درمان بر اساس لنفوسیت های نفوذ کننده به تومور (tumor-infiltrating lymphocytes) در حال حاضر برای حداقل 20 نفر در ایالات متحده مبتلا به ملانوم پیشرفته آماده می شود.
وبینار راهنمایی عملی ثبت و نگارش اختراع همراه با پرسش و پاسخ
وبینار راهنمایی عملی ثبت و نگارش اختراع همراه با پرسش و پاسخ
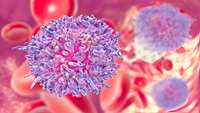
توصیه برای استفاده از روش درمانی مبتنی بر CAR-T برای درمان مولتیپل میلوما بعنوان خط درمانی مقدماتی
کمیته فرآوردههای دارویی برای استفاده انسانی در آژانس دارویی اروپا (CHMP) توصیه کرد که رگلاتوریها Carvykti (ciltacabtagene autoleucel) را به عنوان خط دوم درمان برای بیماران عودکننده یا مقاوم به درمان مولتیپل میلوما تایید کنند. این کمیته به طور خاص تایید درمان سلول های CAR-T با هدایت آنتی ژن بلوغ لنفوسیت B (BCMA) را برای بیمارانی که یک عامل تعدیل کننده سیستم ایمنی و یک مهارکننده پروتئازوم دریافت کرده اند و سرطان آنها نسبت به عامل تعدیل کننده ایمنی Revlimid (لنالیدومید) بریستول-مایرز اسکوئیب مقاوم است، توصیه کرد.
تانیا پلاست فناوری،تولید کننده لوله کشت سلول
به گزارش روابط عمومی و امور بین الملل ستاد توسعه فناوری های پزشکی بازساختی و سلول های بنیادی، جلسه ای پیرامون بررسی پیشرفت پروژه های مورد حمایت این ستاد، مورخ شنبه 11/01/1403 با حضور دکتر عارفیان دبیر ستاد و دکتر دهقانی مدیر گروه منابع انسانی و ترویج با مدیران شرکت تانیا پلاست فناوری در محل شرکت برگزار گردید.
تایید درمان جدید CAR T-Cell برای سرطان کولورکتال به عنوان داروی Orphan از سوی FDA
A2B530 یک گیرنده آنتی ژن کایمریک (CAR) برای درمان با کمک سلول T است که توسط A2 Biotherapeutics برای درمان بیماران مبتلا به سرطان کولورکتال HLA-A*02 مثبت هتروزیگوت با بیان آنتی ژن کارسینوامبریونیک و از دست دادن بیان HLA-A*02 توسعه یافته است.
صدور تاییدیه FDA برای اولین درمان مبتنی بر CAR T-Cell برای بزرگسالان مبتلا به لوسمی یا لنفوم
سازمان غذا و داروی ایالات متحده (lisocabtagene maraleucel [liso-cel]) Bristol Myers Squibb's Breyanzi را به عنوان اولین درمان سلول T با گیرنده آنتی ژن کایمریک (CAR) با هدایت CD19 برای بیماران بزرگسال مبتلا به لوسمی لنفوسیتی مزمن عودکننده یا مقاوم به درمان (CLL) یا لنفوم لنفوسیتی کوچک (SLL) تایید کرده است.
دهقانی در پیام نوروزی تاکید کرد
فراهم بودن زمینههای مشارکت مردم در عرصه تولید و اقتصاد دانشبنیان
معاون علمی، فناوری و اقتصاد دانشبنیان رییسجمهور در پیام نوروزی خود با اشاره به تحولات و اقداماتی که در دوره جدید فعالیت معاونت صورت گرفته، مانعزدایی و هموار کردن مسیر مشارکت شرکت های دانش بنیان و مردم در عرصه تولید و رونق اقتصاد دانشبنیان را از مهمترین رویکردهای معاونت در این دوره عنوان کرد.
بازدید از مرکز نوآوری سلول های بنیادی و پزشکی بازساختی دانشگاه صنعتی شریف
ه گزارش روابط عمومی ستاد توسعه فناوری های پزشکی بازساختی و سلول های بنیادی، دکتر احسان عارفیان به همراه جمعی از مدیران ستاد در تاریخ ۲۰ اسفند ماه ۱۴۰۲ از محل مرکز نوآوری سلول های بنیادی و پزشکی بازساختی دانشگاه صنعتی شریف بازدید کرد.
سلول درمانی CAR-T برای درمان لوپوس
یک مطالعه پیشگامانه فاز 1 با استفاده از سلولهای CAR-T برای درمان لوپوس شدید، تلاش مشترک بین مطالعات سلول درمانی و روماتولوژی را برای پیشگامی در مراقبتهای نوآورانه از بیمار نشان میدهد. بر اساس یک بیانیه مطبوعاتی، Atlantic Health System درمان پیشگامانه ای را برای اولین بیمار در سراسر کشور به عنوان بخشی از مطالعه ارزیابی اثربخشی سلول های گیرنده آنتی ژن کایمریک (CAR-T) در درمان لوپوس آغاز کرد. این مطالعه فاز 1 چند مرکزی، بر روی افراد مبتلا به لوپوس اریتماتوز سیستمیک شدید و مقاوم (SLE) تمرکز دارد.