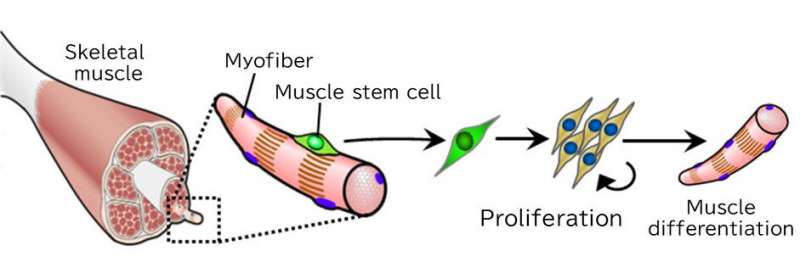
سلول های بنیادی عضله تکثیر می شوند و میوفیبرهای جدید تولید می کنند
یک تیم تحقیقاتی مستقر در دانشگاه کوماموتو، ژاپن کشف کرده است که عضلات و سلول های بنیادی ساکن (سلول های ماهواره ای) مسئول بازسازی عضلات، حافظه ای از اطلاعات محل قرارگیری خود در بدن را نگهداری می کنند.
یک تیم تحقیقاتی مستقر در دانشگاه کوماموتو، ژاپن کشف کرده است که عضلات و سلول های بنیادی ساکن (سلول های ماهواره ای) مسئول بازسازی عضلات، حافظه ای از اطلاعات محل قرارگیری خود در بدن را نگهداری می کنند. مشخص شد که این حافظه موضعی بر اساس الگوی بیان ژن های سراگردان (homeobox) خوشه ژن Hox است که وظیفه شکل دادن به بدن را در طول زندگی جنین بر عهده دارد. انتظار می رود این یافته ها سرنخی برای روشن شدن علت بیماری های عضلانی مانند دیستروفی عضلانی، که در آن موقعیت آسیب پذیری عضله بسته به نوع عضله متفاوت است و به توسعه داروهای احیای ماهیچه مبتنی بر حافظه موضعی کمک کند.
انواع مختلفی از بیماری عضلانی علاج ناپذیر وجود دارند که دیستروفی عضلانی هستند و هر نوع دارای علائم موضعی متفاوتی می باشند. به همین ترتیب، شکنندگی عضله مربوط به سن (سارکوپنی) به طور مساوی در سراسر بدن اتفاق نمی افتد. علائم مکان فیزیکی این بیماریها را نمی توان تنها با تفاوت در انواع فیبرهای عضلانی یا الگوی فعالیتهای بدنی توضیح داد و روشن ساختن پاتوژنزهای مربوطه آنها نیاز به دیدگاه جدیدی دارد.
منشا رشد سلولهایی که عضلات را تشکیل می دهند در مرحله جنینی متفاوت است. به عنوان مثال، بیشتر عضلات جمجمه و صورت از مزودرم جمجمه منشاء می گیرند، در حالی که عضلات اندام ها از سگمنت های بدن منشاء می گیرند. رشد عضلات اندام ها، جمجمه و صورت در دوره جنینی شامل مکانیسم های خاص مولکولی است که به منشاء آنها بستگی دارد. با این حال، تفاوت در ویژگی های عضله اسکلتی بالغ بسته به موقعیت بدن پس از تولد به طور کامل مورد بحث قرار نگرفته است. بنابراین، یک همکاری تحقیقاتی برای تجسم اطلاعات موقعیتی بدن با مطالعه وضعیت اپی ژنومیک و الگوهای بیان ژن عضله اسکلتی و سلولهای بنیادی عضله که مسئول بازسازی هستند، انجام شد.
سلولهای بنیادی عضله که از اندام تحتانی جدا شده و از طریق خارج رحمی به سر پیوند می شوند، باعث می شوند عضلات جمجمه و صورت حافظه موضعی اندام تحتانی را بدست آورند.
محققان با استفاده از عضله اسکلتی و سلولهای بنیادی عضله وابسته جدا شده از سر و اندامهای تحتانی موشهای بالغ، ویژگی موقعیتی را در سطح اپی ژنومیک با استفاده از تجزیه و تحلیل متیلوم DNA بررسی کردند. آنها تفاوت های اختصاصی را در وضعیت متیلاسیون DNA در مکان های ژنی Hox پیدا کردند. در میان چهار منطقه ، A تا D ، به طور خاص مکان ژنی Hox-A دارای یک حالت کلی هیپرمتیلاسیون DNA در عضلات اسکلتی اندام تحتانی و سلولهای بنیادی عضله در مقایسه با سر است. علاوه بر این، هر دو عضله اسکلتی و سلولهای بنیادی عضله در اندام های تحتانی بیان بالایی از ژن Hox-A را نشان دادند. بسیاری از این ژن های Hox-A الگوهای بیان را در دوره جنینی منعکس می کنند. این یافته ها نشان می دهد که عضلات اسکلتی و سلولهای بنیادی عضله اطلاعات موضعی را در طول زندگی جنین به یاد می آورند و تنظیم اپی ژنومی توسط متیلاسیون DNA ممکن است در حافظه موضعی نقش داشته باشد.
محققان سپس بر روی ژن Hoxa10 متمرکز شدند که فقط در عضلات اندام ها بیان می شود. هنگامی که سلولهای بنیادی عضله مشتق از اندام تحتانی بیان کننده Hoxa10 جدا شده و به عضلات جمجمه و صورت که بیان کننده Hoxa10 نیستند پیوند داده می شوند، بیان ژن Hoxa10 در عضلات جمجمه و صورت قابل تشخیص است. به عبارت دیگر، سلولهای بنیادی عضله اندام تحتانی قادر به عصب کشی عضله جمجمه و صورت با حفظ قدرت حافظه موضعی حتی پس از پیوند خارج رحمی هستند.
آنها سپس موش هایی فاقد ژن Hoxa10 در سلول های بنیادی عضله را برای تجزیه و تحلیل عملکرد آن ایجاد کردند. کمبود Hoxa10 بازسازی عضلات اندام تحتانی را به شدت مختل می کند اما تاثیری در بازسازی عضلات جمجمه و صورت ندارد. یک بررسی دقیق از مکانیسم اختلال بازسازی عضله اندام حرکتی تحتانی نشان داد که علت آن بی ثباتی ژنومی به دلیل توزیع غیر طبیعی کروموزوم در طول تقسیم سلول های بنیادی عضله است. بعلاوه تجزیه و تحلیل سلولهای بنیادی عضله سر و پا انسان نیز نشان داد که فقط سلولهای عضلانی پا ژن HOX-A را بیان می کنند و مهار آن منجر به تقسیم سلولی غیرطبیعی می شود و این امر تأیید می کند که حافظه موضعی سلول عضلانی در انسان و موش حفظ می شود.
این تحقیقات نشان می دهد که حافظه موضعی سلولهای بنیادی عضله بر اساس توزیع موقعیت خاص بیان ژن Hox ممکن است ویژگی های خاص موقعیت عضله اسکلتی را تعیین کند.
دانشیار یوسوکه اونو، گفت:"در آینده، ما انتظار داریم که جنبه های عملکردی حافظه موضعی سلول های بنیادی عضله منجر به روشن شدن مکانیزمی شود که منجر به علائم اختصاصی موضعی می شود که در بیماری های مختلف عضلانی مانند دیستروفی عضلانی مشاهده می شود. علاوه بر این، آزمایش های پیوند خارج رحمی که در آن سلول های بنیادی عضله به مکانی متفاوت از محل برداشته شده، پیوند می شوند، نشان داده است که آنها حافظه موضعی را حفظ می کنند و ماهیچه را از نو تولید می کنند."
از دیدگاهی دیگر، عضلات اسکلتی که از طریق پیوند بیگانه (Xenotransplantation) تولید شده اند ممکن است اطلاعات موضعی اصلی خود را نداشته باشند که ممکن است عملکرد طبیعی آنها را مختل کند. اخیراً در تمایز سلولهای iPS به سلولهای مختلف مولد و توسعه روشهای کشت انبوه پیشرفت سریعی صورت گرفته است، اما محل سلولهای پیش ساز القایی در نظر گرفته نشده است. در آینده، گروه ما تلاش خواهد کرد تا با کنترل مصنوعی حافظه موضعی سلولها و با استفاده از خواص سلولهای دارای حافظه موضعی در مکانهای مناسب، برنامه های درمانی احیا کننده را برای بیماریهای عضلانی توسعه دهد."
https://medicalxpress.com/news/2021-07-muscles-retain-positional-memory-fetal.html



ارسال به دوستان