تسهیل تمایز سلولهای PSC انسان به سلولهای کبدی بالغتر توسط گیرنده هستهای THRB
پژوهشگران به منظور درک مکانیسمهای تنظیم کننده بلوغ آزمایشگاهی سلولهای کبدی مشتق از hPSC، یک سیستم تمایز سهبعدی ایجاد کردند و عناصر تنظیمکننده ژن را در سلولهای کبدی اولیه انسان با سلولهای کبدی-hPSC که در شرایط دو بعدی یا سه بعدی توسط RNA-seq، ATAC. -seq و H3K27Ac ChiP-seq تمایز یافتند، مقایسه کردند.
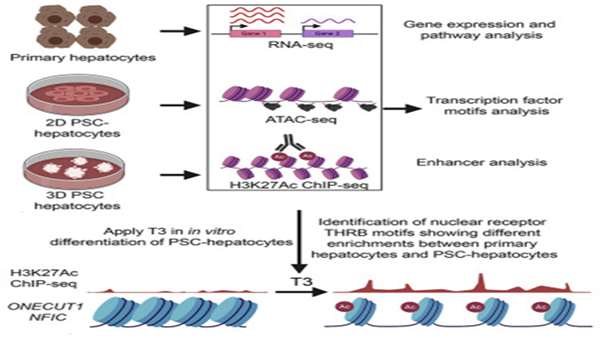
پژوهشگران به منظور درک مکانیسمهای تنظیم کننده بلوغ آزمایشگاهی سلولهای کبدی مشتق از hPSC، یک سیستم تمایز سهبعدی ایجاد کردند و عناصر تنظیمکننده ژن را در سلولهای کبدی اولیه انسان با سلولهای کبدی-hPSC که در شرایط دو بعدی یا سه بعدی توسط RNA-seq، ATAC. -seq و H3K27Ac ChiP-seq تمایز یافتند، مقایسه کردند. مقایسههای رگولوم، کاهش تقویت موتیفهای THRB گیرنده تیروئید در کروماتین در دسترس و تقویتکنندههای فعال را بدون کاهش رونویسی THRB نشان داد. افزودن هورمون تیروئید T3، اتصال THRB به تقویتکننده پروگزیمال CYP3A4 را افزایش داد.
وضعیت فوق تقویت کننده و بیان ژن NFIC را بازسازی کرد و بیان AFP را کاهش داد. سلولهای کبدی hPSC حاصل، بیان ژن، وضعیت اپیژنتیک و چشمانداز فوق تقویتکننده نزدیکتری را به سلولهای کبدی اولیه و مناطق تنظیمکننده فعال از جمله SNP های غیرکدکننده مرتبط با بیماریهای مرتبط با کبد نشان دادند. پیوند هپاتوسیتهای hPSC منجر به پیوند سلولهای کبدی انسان به کبد موش، بدون ایجاد اختلال در بافتشناسی طبیعی کبد شد. این کار محوریت عامل محیطی-گیرنده هستهای را در تنظیم بلوغ سلولهای کبدی hPSC نشان میدهد.
https://doi.org/10.1016/j.stem.2022.03.015



ارسال به دوستان