تبدیل مستقیم سلول های بنیادی مزانشیمی بند ناف انسان به سلول های اپیتلیال رنگدانه شبکیه به منظور درمان دژنراسیون (تحلیل رفتگی)شبکیه
دژنراسیون ماکولار وابسته به سن (AMD) یکی از علل اصلی اختلال بینایی در سراسر جهان است. این بیماری از طریق صدمه به عملکرد بینایی ناشی از آپوپتوز و از دست رفتن عملکرد سلولهای اپیتلیال رنگدانه شبکیه (RPE) و سلولهای گیرنده نور شبکیه مشخص میشود .
دژنراسیون ماکولار وابسته به سن (AMD) یکی از علل اصلی اختلال بینایی در سراسر جهان است. این بیماری از طریق صدمه به عملکرد بینایی ناشی از آپوپتوز و از دست رفتن عملکرد سلولهای اپیتلیال رنگدانه شبکیه (RPE) و سلولهای گیرنده نور شبکیه مشخص میشود AMD . اغلب منجر به اختلال شدید بینایی و در نهایت نابینایی میشود که به طور جدی بر کیفیت زندگی بیماران تأثیر میگذارد. در سالهای اخیر، درمانهای مبتنی بر سلولهای بنیادی در کلینیک به کار گرفته شده اند و نتایج درمانی مشهودی را نشان میدهند.
محققان نشان داده اند پیوند سلولهای بنیادی مزانشیمی(MSC) به فضای زیر شبکیه میتواند به طور قابل توجهی آپوپتوز سلول گیرنده نوری را مهار کند و از دست دادن بینایی را در مدل AMD حیوانی به تاخیر بیندازد. با این حال، توانایی تمایز سلولهای بنیادی مزانشیمی پیوند شده به فضای زیر شبکیه در مدلهای AMD رت همچنان بحث برانگیز بوده و محل پیوند نیز بر نتایج روش درمانی مبتنی بر MSC برای بیماری دژنراسیون شبکیه تأثیر میگذارد. بنابراین انتظار میرود ، تمایز سلولهای بنیادی مزانشیمی به سلولهای RPE در شرایط آزمایشگاهی و سپس پیوند آن به فضای زیر شبکیه، نتیجه سلول درمانی را بهبود بخشد.
مولکولهای کوچک و یا محیط کشت مجاور شده با سلول های RPE به منظور القای تمایز سلولهای بنیادی مزانشیمی به سلول های RPE در شرایط آزمایشگاهی مورد استفاده قرار گرفتند. در حالی که محیط شبکیه چشم بیماران AMD نامطلوب است. شواهد بالینی نشان میدهند سلولهای RPE در افراد مبتلا به AMD تحت گذر از حالت اپیتلیالی به حالت مزانشیمی (EMT) قرار میگیرند و TGF-β(transforming growth factor-β) ، یک القاگر EMT، در شبکیه بیماران AMD در مقایسه با چشمان نرمال افراد گروه کنترل افزایش مییابد. این مهم نشان میدهد به احتمال فراوان سلولهای RPE پیوندی بدست آمده از سلولهای بنیادی مزانشیمی تحت EMT قرار میگیرند و متعاقباً اثر درمانیشان کاهش مییابد. بنابراین، اگر سلولهای RPE مشتقشده از سلولهای بنیادی مزانشیمی قابلیت anti-EMT از خود بروز دهند، اثربخشی درمانهای مبتنی بر MSC بسیار بهبود مییابد.
گزارش شده است که فاکتورهای رونویسی کلیدی میتوانند یک نوع سلول را به دودمان دیگری از سلولها تمایز دهند.(دگرتمایزی)
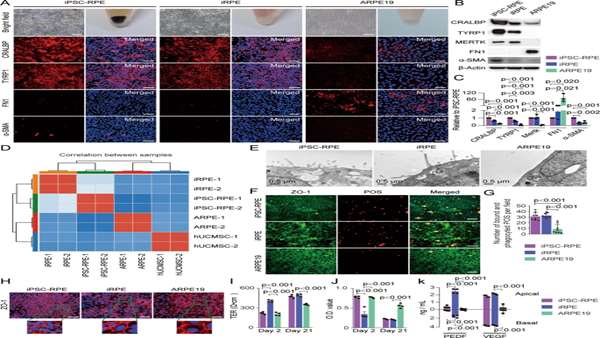
بر اساس این شواهد، محققان ترکیبی از فاکتورهای رونویسی کلیدی که قادر به تمایز سلولهای بنیادی مزانشیمی بند ناف انسان(hUCMSC) به سلولهای RPE-like به نام سلولهای RPE القایی (iRPE) بودند را ارزیابی کردند. سلولهای hUCMSC توسط پنج فاکتور رونویسی کلیدی به سلول های iRPE متمایز شدند: CRX، NR2E1، C-MYC، LHX2، و SIX6.
سلولهای iRPE دارای ویژگیهای قابل مقایسه با سلولهای RPE بدست آمده از سلولهای بنیادی پرتوان القایی (iPSC-RPE) میباشند و خواص anti-EMT دارند. الگوهای بیان ژن و عملکرد سلولهای iRPE مشابه سلولهای iPSC-RPE است و سلولهای iRPE به طور قابل توجه عملکرد درمانی بهتری نسبت به hUCMSC ها دارند.
تصور میشود CRX فاکتور رونویسی کلیدی به منظور تعیین سرنوشت سلولهای گیرنده نوری است و C-MYC نقش مهمی را در کنترل تکثیر سلولی، رشد، تمایز، آپوپتوز، بقا و خود نوزایی سلولهای بنیادی ایفا میکند. LHX2 بیان ژنهای چرخه بینایی را در سلولهای RPE تنظیم میکند. LHX2 و C-MYC برای حفظ عملکرد RPE بالغ ضروری هستند.
محققان تأیید کردهاند که پیوند سلولهای iRPE مشتق از hUCMSC ها بهطور قابلتوجهی نتایج درمانی را در مدل حیوانیAMD بهبود میبخشد، که ارزش کاربرد بالینی hUCMSC ها را افزایش میدهد.
محدودیت مطالعه صورت گرفته آن است که محققان از رتروویروسها برای ادغام ژنوم پنج فاکتور رونویسی ذکر شده در کروموزوم hUCMSC ها به منظور باز برنامهریزی سلولها به سلولهای iRPE استفاده کرده اند. اگرچه پس از پیوند سلولهای iRPE در موشهای nude تومورزایی مشاهده نشد، اما همچنان در مورد استفاده بالینی در آینده ریسک فاکتورهای احتمالی وجود دارد.
علاوه بر این، با توجه به آنکه تعداد زیادی از سلولهای پیوند شده 6 هفته پس از پیوند مردند، یک طرح سرکوب ایمنی مناسب برای طولانی کردن بقای سلول های پیوند شده در مدل های حیوانی مورد نیاز است.
منبع :



ارسال به دوستان