آنتی بادی مونوکلونال هدف گیرنده میلوما، امید جدیدی را برای درمان مولتیپل میلوما ارائه می دهد
مولتیپل میلوما (MM) یک سرطان غیرقابل درمان سلول های پلاسما با پیش آگهی بسیار ضعیف است. با این حال، محققان ژاپنی اخیرا دریافتهاند که یک جزء مشترک از ناقلهای اسید آمینه، زنجیره سنگین CD98، یک هدف آنتیبادی مونوکلونال موثر در درمان MM را نشان میدهد
مولتیپل میلوما (MM) یک سرطان غیرقابل درمان سلول های پلاسما با پیش آگهی بسیار ضعیف است. با این حال، محققان ژاپنی اخیرا دریافتهاند که یک جزء مشترک از ناقلهای اسید آمینه، زنجیره سنگین CD98، یک هدف آنتیبادی مونوکلونال موثر در درمان MM را نشان میدهد.
در مطالعهای که این ماه در Science Translational Medicine منتشر شد، محققان دانشگاه اوزاکا رویکرد جدیدی را نشان دادند که شامل غربالگری گسترده کلونهای آنتیبادی مونوکلونال در برابر نمونههای تومور اولیه انسانی است. هدف شناسایی اپی توپ های ساختاری اختصاصی سرطان بر روی پروتئین ها بود که با آنالیز ترنسکریپتوم یا پروتئوم قابل شناسایی نیستند.
برخی از بیماران مبتلا به MM عود بیماری را نشان می دهند که اغلب به دلیل جهش های گریزنده از سیستم ایمنی ایجاد می شود که سلول های سرطانی را در برابر درمان مقاوم می کند. بنابراین آنتی ژن های هدف جدید برای ایجاد یک رویکرد چند هدفه که بتواند فرار از سیستم ایمنی را دور بزند و در نتیجه از عود بیماری جلوگیری کند، شدیدا مورد نیاز است.
تلاشهای گسترده قبلی بر روی هدف قرار دادن آنتی ژنهای سطح سلولی اختصاصی سرطانی که با آنالیز ترنسکریپتوم یا پروتئوم شناسایی شدهاند، متمرکز شدهاند. اما این تلاشها ممکن است اپیتوپهای آنتیژن اختصاصی سرطانی را که توسط اصلاح کووالانسی و آنزیمی پروتئینها (یعنی تغییرات پس از ترجمه)، مانند گلیکوزیلاسیون یا تغییرات ساختاری تشکیل شدهاند، از دست داده باشد. هاسگاوا و همکارانش برای گسترش جستجو برای آنتی ژن های هدف جدید، آنتی بادی های مونوکلونال مخصوص سرطان را غربالگری کردند و سپس آنتی ژن های ارائه دهنده هدف آنها را مشخص کردند.
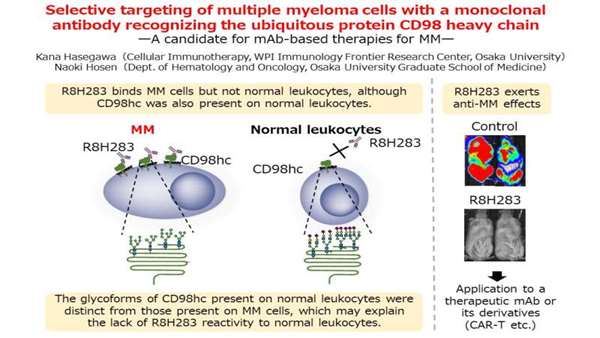
کانا هاسگاوا، سرپرست تیم تحقیق، میگوید: «با غربالگری بیش از 10000 کلون آنتیبادی مونوکلونال ایجاد شده علیه سلولهای MM، R8H283، یک آنتیبادی مونوکلونال را شناسایی کردیم که پروتئین زنجیره سنگین CD98 را که بخشی از یک ناقل اسید آمینه است، تشخیص میدهد». علیرغم وجود زنجیره سنگین CD98 روی همه سلول ها، آنتی بادی فقط به سلول های MM متصل می شود. این گزینش پذیری ممکن است منعکس کننده الگوهای مختلف گلیکوزیلاسیون بین سلول های طبیعی و سلول های MM باشد.
تجزیه و تحلیل عمیق آنتی بادی R8H283 اتصال ویژه به هترودایمرهای CD98، نه مونومرهای زنجیره سنگین CD98 را نشان داد. کمپلکس های هترودایمر که شامل زنجیره سنگین CD98 و زنجیره سبک هستند، جذب اسیدهای آمینه را برای تولید ایمونوگلوبولین تعدیل می کنند. نائوکی هوسن، نویسنده ارشد این مقاله توضیح میدهد: «جالب است که گلیکوفرمهای زنجیره سنگین CD98 در هترودیمرهای موجود در لکوسیتهای طبیعی از گلیکوفرمهای موجود در سلولهای MM متمایز بودند، که فکر میکنیم فقدان واکنش R8H283 به لکوسیتهای طبیعی را توضیح میدهد». "این رخداد بسیار مهم است زیرا به این معنی است که آنتی بادی R8H283 می تواند اثرات ضد MM را بدون آسیب رساندن به سلول های میزبان عادی اعمال کند."
برای ارزیابی اثربخشی آنتی بادی R8H283 در یک مدل حیوانی، محققان از مدل زنوگرافت MM موشی استفاده کردند. آنها دریافتند که تزریق R8H283 بقای موش ها را طولانی تر می کند. این تایید کرد که R8H283 کاندیدای درمان مبتنی بر آنتی بادی مونوکلونال برای MM است.
نهایتا، این یافتهها رویکرد مؤثری را برجسته میکنند که به وسیله آن اپی توپهای ساختاری اختصاصی سرطان روی پروتئینهایی که با آنالیز ترنسکریپتوم یا پروتئوم قابل شناسایی نیستند، از طریق غربالگری نمونههای تومور اولیه شناسایی میشوند. این روش ممکن است در گسترش آرایه آنتی ژن های سطحی اختصاصی سرطان موجود برای توسعه دارو در آینده مفید باشد.
https://medicalxpress.com/news/2022-02-myeloma-targeting-monoclonal-antibody-multiple-myeloma.html



ارسال به دوستان