تحقیقات جدید جهت غلبه بر تومورهای جامد با ایمونوتراپی سلول های CAR T
درمان با سلول T CAR، روشی نوآورانه برای فعال کردن سلول های T بیماران در آزمایشگاه برای حمله به سرطان پس از تزریق مجدد، در برابر سرطان های خون مؤثرتر از تومورهای جامد عمل کرده است.
درمان با سلول T CAR، روشی نوآورانه برای فعال کردن سلول های T بیماران در آزمایشگاه برای حمله به سرطان پس از تزریق مجدد، در برابر سرطان های خون مؤثرتر از تومورهای جامد عمل کرده است.
اکنون، در تحقیقات جدید با هدف یافتن دلیل و چگونگی غلبه بر مشکل در تومورهای جامد، دانشمندان در میلان ایتالیا کشف کرده اند که تومورهای جامد خود را در یک پوشش قندی محافظت میکنند که آنها را در برابر حمله سلولهای CAR T مقاوم میکند . بئاتریس گرکو و همکارانش در واحد ایمنی درمانی نوآورانه در موسسه علمی IRCCS San Raffaele در حال بررسی راه هایی برای غلبه بر آن هستند. آنها در حال ابداع مولکولی هستند که بتواند سپر قندی را بشکند، که به نوبه خود مسیری را برای سلول های CAR T باز می کند تا به محیط توموری بروند و سرطان های جامد را از بین ببرند.
سلول های CAR T - سلول های T بیان کننده گیرنده آنتی ژن کایمریک - نخست سلول های T خود بیمار هستند که نمونه خون جداسازی می شوند. در مرحله بعد، سلولها در آزمایشگاه با استفاده از یک فرآیند اصلاح ژنتیکی تغییر داده میشوند که باعث میشود سلولهای T یک گیرنده جستجوگر و نابودکننده سرطان را روی سطح خود بیان کنند.
علیرغم سالها تحقیق، با وجود تلاش دانشمندان علوم پزشکی تاکنون موفق نشده اند که سلولهای T فعال را به همان اندازه که برای بدخیمیهای خونی کارآمد هستند، در برابر تومورهای جامد مؤثر کنند. و گلیکوزیلاسیون سطح سلول سرطانی، فرآیند تقویت سلول های سرطانی در پوشش ضخیمی از مولکول های قند، به مشکلاتی در استفاده از CAR T در برابر انواع تومورهای جامد منجر شده است.
مطالعات آزمایشگاهی شامل مدل های حیوانی نشان میدهد که راهحلی برای مشکل سپر قندی ممکن است در آیندهای نه چندان دور به آزمایش های بالینی انسانی راه پیدا کند.
گرکو در «Science Translational Medicine» نوشت: «ایمونوتراپی با سلولهای T مهندسیشده توسط گیرنده آنتیژن کایمریک موفقیت های استثنایی را در بیماران مبتلا به بدخیمی های مقاوم به سلول B نشان داد. "با این حال، اولین مطالعات در انسان روی تومورهای جامد، موانع منحصر به فردی را نشان داد که به اثربخشی ضعیف کمک می کند. درک عوامل تعیین کننده تشخیص تومور توسط سلول های CAR T باید به طراحی استراتژی هایی تبدیل شود که می توانند بر مقاومت موجود غلبه کنند."
فقط یک مشکل سپر قندی نیست که از کارکرد سلول درمانی CAR T در تومورهای جامد جلوگیری می کند، اگرچه پوشش کربوهیدراتی بزرگترین مانع برای درمان موفقیت آمیز بوده است. ریزمحیط تومورهای جامد از نفوذ مناسب سلول های CAR T در محل تومور جلوگیری می کند. علاوه بر این، تومورهای جامد همچنین دارای آنتی ژن های کمی هستند که سلول های CAR T می توانند به راحتی آن ها را تشخیص دهند و آن را به صفر برسانند.
گفته شده است که محققان در سراسر جهان در حال کار بر روی راه هایی برای غلبه بر این موانع هستند، اما به گفته دانشمندان در میلان، کار بیشتری برای درک عوامل موثر بر شناسایی هدف بدخیم توسط سلول های CAR T و تعامل با آن، مورد نیاز است.
برای اینکه بدانند چرا تقریباً هر نوع تومور جامد به درمان با سلول های CAR T مقاوم است، گرکو و همکارانش به دنبال ویژگی مشترک این سرطان ها در مورد محافظت از سلول های خود در برابر تخریب شدند. این تیم دریافت که "کارسینوم های متعدد N-گلیکان های خارج سلولی را بیان می کنند، که فراوانی آنها با توانایی کشندگی سلول های CAR T ارتباط منفی دارد."
گلیکوزیلاسیون N-linked به یک فرآیند شیمیایی مهم اشاره دارد که در آن یک الیگوساکاریل ترانسفراز (یک آنزیم) انتقال یک الیگوساکارید را به یک گیرنده اسید آمینه، که در این مورد آسپاراژین است، کاتالیز می کند. الیگوساکارید کربوهیدراتی است که از رشته ای از زیر واحدهای مونوساکارید تشکیل شده است.
این را به عنوان فرآیندی از ساخت یک زنجیره با چندین واحد، که بارها و بارها به هم مرتبط میشوند، تصور کنید. هر بار که یک الیگوساکارید به آسپاراژین در معرض متصل می شود حلقه دیگری در زنجیره ایجاد می کند. نتیجه نهایی این است که زنجیرهای محکم از مولکول های قند که سپری روی سلول های سرطانی ساخته اند. در سطح کلان، تومور در قندهایی احاطه می شود که سرطان را از حمله محافظت می کند. گرکو و همکارانش می گویند گلیکوزیلاسیون مرتبط با N کلید مقاومت تومورهای جامد در برابر ایمونوتراپی سلول های CAR T است.
گرکو و همکارانش دریافتند که با گنجاندن یک آنالوگ قند - یک مولکول ضد قند که به عنوان سپر مقابل عمل می کند - به همراه سلول های CAR T، می توان قدرت کشندگی سلول های T فعال شده را افزایش داد. و از آنجایی که سلول های سرطانی روش های زیادی برای فرار از هر نوع درمانی دارند، او و تیمش میگویند که ترکیب مولکول ضد قند در درمان های سلول های CAR T میتواند به غلبه بر ترفندهای متعددی که تومورها ممکن است برای محافظت از خود استفاده کنند، کمک کند.
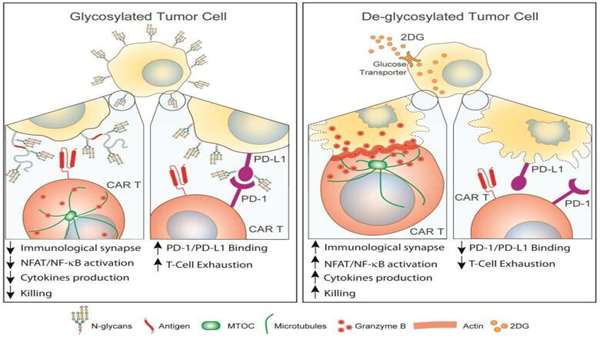
گرکو نوشت: "ما نشان دادیم که N-گلیکان ها با تداخل در تشکیل سیناپس ایمونولوژیک مناسب و کاهش فعال سازی رونویسی، تولید سیتوکین و سمیت سلولی، تومورها را از کشندگی سلول های CAR T محافظت می کنند." "برای غلبه بر این مانع، ما از تقاضای متابولیک بالای تومورها برای مهار ایمن سنتز N-گلیکان ها استفاده کردیم."
سلولهای لوزالمعده در ترکیبات کربوهیدراتی - N-گلیکانها - در سطح خود به طرز چشمگیری محافظت میکنند. N-گلیکان ها به عنوان یک نیرو در برابر سلول های CAR T در سرطان پانکراس عمل می کنند. این بدخیمی یکی از سخت ترین سرطان ها برای درمان است. امکان استفاده از ایمونوتراپی با سلول های CAR T می تواند به امیدی که پزشکان ممکن است روزی به آن تکیه کنند اضافه کند.
برای حل مشکل پوشش قندی، این تیم از یک عامل مولکولی - یک 2-دئوکسی-D-گلوکز - یک آنالوگ قند استفاده کردند که می تواند سنتز N-گلیکان ها را مهار کند. محققان دریافتند که درمان تومورهای لوزالمعده در موشها با 2-دئوکسی-D-گلوکز باعث شکسته شدن پوشش محافظ N-گلیکان سلول های توموری شده و آنها را نسبت به درمان با سلولهای CAR T آسیبپذیرتر میکند.
علاوه بر این، درمان ترکیبی (2-دئوکسی-D-گلوکز به اضافه ایمونوتراپی سلول CAR T) همچنین طیفی از تومورهای جامد دیگر را به درمان با سلول های CAR T حساس کرد. این تومورهای جامد شامل سرطان ریه، تخمدان و مثانه بودند.
در حالی که محققان در میلان و فراتر از آن در حال کار بر روی راههایی برای غلبه بر موانع توانایی سلولهای CAR T برای از بین بردن سرطانها هستند، برای درک عواملی که بر اینکه آیا یک سلول CAR T میتواند هدف بدخیم خود را شناسایی کرده و با آن تعامل داشته باشد، به کار بیشتری نیاز است.
برای بهبود شانس موفقیت درمان، دانشمندان پزشکی در آزمایشگاههای سراسر جهان به دنبال راههایی هستند تا درمان سرطان سلولهای CAR T را برای سرطانهای هماتولوژیکی و جامد مؤثرتر کنند.
گرکو گفت: «به طور کلی، نتایج ما نشان میدهد که N-گلیکوزیلاسیون تومور، کیفیت و میزان پاسخ های سلول های CAR T را تنظیم میکند و راه را برای طراحی منطقی درمانهای بهبود یافته در برابر بدخیمی های جامد هموار میکند.
https://medicalxpress.com/news/2022-03-car-cell-immunotherapy-solid-tumors.html



ارسال به دوستان